Bringer medisin rett til kreftcellene og sparer friske celler
En ny behandlingsmetode for kreft kombinerer ultralyd, bobler og nanopartikler med cellegift. I forsøk har metoden kurert kreft hos mus.
En tredjedel av alle nordmenn vil oppleve å bli kreftsyke. Det gjelder omlag en og halv million av oss. I tillegg rammes mange pårørende som må leve med sykdommen tett innpå livet.
En god del av dem som får kreft, opplever heldigvis i dag å bli friske, og en av de grunnleggende behandlingsmetodene er cellegift. Men prisen for cellegiftbehandling er høy. Under behandlingen sprer cellegiften seg til alle cellene i kroppen, også de som er friske. Dermed ødelegges friske celler, og mange sliter med store bivirkninger under og etter behandling.
Et annet viktig moment: Når alle cellene skal ”dele på medisinen”, er det bare 0.01 prosent av cellegiftdosen som når fram til svulsten med de syke cellene.
– Jeg jobber med å finne ut hvordan vi skal få fraktet mer cellegift fram til svulsten og mindre til de friske cellene, sier Sofie Snipstad, som nylig avla sin doktorgrad ved Institutt for fysikk ved NTNU. For snart ett år siden vant hun Forsker Grand Prix, og da hun presenterte forskningen sin under finalen, sto hun midt oppe i de første testene av en ny metode for kreftbehandling. Testene ble gjort på mus.
Nå viser testene at metoden kurerer kreft hos mus.
Lovende resultater
Metoden går ut på å bringe cellegift målrettet fram til kreftsvulstene slik at det kommer mest mulig medisin fram til de syke kreftcellene og at de friske cellene spares. Forsøkene som ble gjort i musene, ble testet på en aggressiv brystkrefttype (trippel-negativ).
Forskere gjorde mange forsøk i laboratoriet i forkant av musetestene – som var de første reelle testene av denne metoden å distribuere medisin på. Resultatene er løfterike.
I tillegg til at svulstene forsvant under behandlingen, viser forsøkene at kreften heller ikke er kommet tilbake.
– Dette er spennende teknologi som har vist svært lovende resultater. At de første resultatene i mus er så gode og at medisinen treffer så bra allerede fra starten av, er svært lovende, sier Sofie Snipstad.
Slik fungerer behandlingen
I stedet for at cellegift sprøytes rett inn i blodet og fraktes vilkårlig ru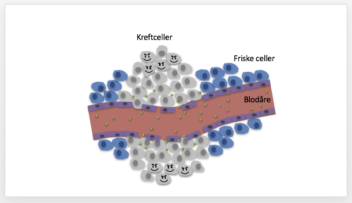 ndt til både syke og friske celler, kapsles medisinen inn i nanopartikler. Når nanopartiklene med medisin sprøytes inn i blodet, er nanopartiklene såpass store at de ikke slipper ut av blodårene i de fleste typer frisk vev. Dermed vil ikke cellegiften skade friske celler.
ndt til både syke og friske celler, kapsles medisinen inn i nanopartikler. Når nanopartiklene med medisin sprøytes inn i blodet, er nanopartiklene såpass store at de ikke slipper ut av blodårene i de fleste typer frisk vev. Dermed vil ikke cellegiften skade friske celler.
I svulsten derimot, har blodårene porøse vegger slik at nanopartiklene med medisin slipper inn til de kreftsyke cellene.
– Jeg har funnet ut at vi med denne metoden kan frakte 100 ganger mer cellegift til svulsten sammenlignet med cellegift alene. Det er bra, sier Sofie Snipstad.
– Men, nanopartiklene når bare ut til de cellene som ligger nærmest blodårene som frakter dem. Kreftceller som ligger langt unna får ingenting. For at

SINTEF-forsker Ýrr Mørch er en av forskerne bak nanokapslene som frakter medisinen inn i blodstrømmen ved hjelp av ørsmå gassbobler og ultralyd. Det gjør at medisinen virker nøyaktig der den skal. Nanokapslene produseres i denne reaktoren i SINTEFs laboratorier. Foto: Christina Benjaminsen.
behandlingen skal være effektiv, er det viktig at behandlingen når ut til hele Derfor trenger nanopartiklene vår hjelp for å få medisinen helt fram, forklarer hun.
Ultralyd er nøkkelen
Nanopartiklene som Sofie Snipstad og forskningsteamet bruker, er utviklet ved SINTEF i Trondheim. De er helt spesielle fordi de kan danne små bobler. Nanopartiklene ligger i skallet til boblene.
Boblene er en viktig del av suksessen. En annen essensiell del, er bruk av ultralyd. Det er primært bruken av ultralyd Sofie Snipstad forsker på.
Boblene med nanopartikler som frakter cellegift, sprøytes inn blodet. Deretter settes ultralyd på svulsten. Ultralyden får boblene til å vibrere og etter hvert sprekke slik at nanopartiklene løsner. Vibrasjonene vil også massere blodårene og vevet slik at det dannes flere porer. Det bidrar til at nanopartiklene dyttes lenger ut i kreftsvulsten, og altså ikke bare slipper fram til de kreftcellene som ligger nærmest blodårene.
– Ved å bruke ultralyd i forbindelse med transport av nanopartikler med cellegift til svulster i mus, har jeg vist at vist at vi kan få levert omtrent 250 ganger mer av dosen til svulsten, enn bare ved å sprøyte inn cellegift alene, forklarer hun.
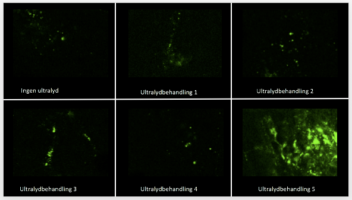
For å få boblene til å oppføre seg som de ville, testet forskerne mange ulike ultralydbehandlinger, og målte hvor mye nanopartikler som ble levert til kreftvev i mus. Mange av ultralybehandlingene hadde liten effekt, men Sofie Snipstad fant én som fungerte svært bra.
Tre grupper, tre tydelige resultater
Musene ble delt inn i tre grupper:
- Gruppe 1 fikk ingen behandling. Kreftsvulsten vokste raskere og raskere.
- Gruppe 2 fikk behandling med nanopartikler med medisin. Veksten til svulsten stagnerte etter en tid, men svulsten forsvant ikke.
- Gruppe 3 fikk behandling med nanopartikler med medisin, bobler og ultralyd. I denne gruppen krympet svulsten helt til den forsvant. 100 dager etter avsluttet behandling, var musene fortsatt kreftfrie.
Må lure kreftcellene
– For at behandlingen skal være effektiv, må vi lure kreftcellene til å spise nanopartiklene slik at cellegiften kommer helt fram til målet, sier Snipstad.
For å studere denne prosessen har hun dyrket kreftceller og studert dem i mikroskop. Det hun har sett, er at nanopartiklene kamuflerer cellegiften og det gjør at kreftcellene spiser cellegift med glede. Men for at behandlingen skal virke, må nanopartiklene gi fra seg cellegiften akkurat hvor og når det trengs.
– Det kan vi gjøre ved å endre den kjemiske sammensetningen i nanopartiklene, slik at vi kan skreddersy egenskaper, blant annet bestemme hvor raskt nanopartiklene skal brytes ned. Etter at nanopartikkelen er spist av cellen, løser nanopartikkelen seg opp og frigir cellegift inne i cellen. Da vil kreftcellen slutte å dele seg, og etter hvert skrumpe inn og dø.
Tett tverrfaglig samarbeid
Forskningsgruppen som Snipstad er en del av, ledes av Catharina Davies. Gruppen jobber i stor grad med nanopartikler, og det var interessen for nanoteknologi som brakte Sofie Snipstad til NTNU og etter hvert inn i forskningsgruppen til Davies.
NTNU-miljøet samarbeider tett med SINTEF og St. Olavs Hospital. NTNU utfører
forsøkene på mus og studerer kreftcellene. SINTEF utvikler boblene med nanopartikler, som er plattformen for forskningen. Kreftklinikken og ultralydmiljøet ved St. Olavs er involvert med sin kliniske kompetanse.
– En av de tingene som jeg setter stor pris på, er at det er så mange flinke mennesker med ulik bakgrunn som er involvert i prosjektet. Trondheim har et veldig bra tverrfaglig miljø, og i dette prosjektet trenger vi alle de involverte fagområdene for at forskningen skal gå framover.
Når kan metoden tas i bruk?
Forskningsresultatene gir altså grunn til optimisme, og så langt har prosessen gått raskt. Likevel er det langt fram til metoden kan tas i bruk i kreftbehandling hos mennesker.
– Fra man gjør en oppdagelse på laboratoriet til den kan tas i bruk, regner man 10-20 år. Vi har jobbet med dette i ca seks år, så det gjenstår mye arbeid ennå. Vi må forstå mer av mekanismene bak dette, og gjennom mikroskopering må vi studere hva som skjer inne i vevet, sier Snipstad og fortsetter:
– Når man får slike lovende resultater som vi har fått, åpner det seg så mange nye dører og så mye man ønsker å forstå og finne ut av! Vi må blant annet teste ut denne metoden på andre tumormodeller, for hvert krefttilfelle er unikt.
Åpner opp for behandling av sykdom i hjernen
Metoden med bobler, nanopartikler og ultralyd åpner også opp for behandling av sykdommer i hjernen. Hjernen vår er svært godt beskyttet på mange vis. Det gjør også at den i stor grad er stengt for å ta i mot behandling.
Hjernens blodårenettverk er ganske ulikt blodårenettverket i svulstene. Hjernen er godt beskyttet mot stoffer som blodet frakter med seg og slipper kun inn stoffer som hjernecellene trenger. Dette kalles blod-hjerne-barrieren, og på grunn av den er det svært vanskelig å levere medisin til hjernen. For mange sykdommer i hjernen finnes det derfor ennå ingen behandling.
– Men det finnes håp. Ved bruk av ultralyd og våre bobler har vi klart å levere nanopartikler og medisin til hjernen. Dette kan være lovende for behandling av kreft og andre sykdommer i hjernen, avslutter Sofie Snipstad.
Studien Ultrasound Improves the Delivery and Therapeutic Effect of Nanoparticle-Stabilized Microbubbles in Breast Cancer Xenografts ble nettopp publisert i Ultrasound in Medicine and Biology.